の TGA 補完医療などのリストされた(低リスク)医薬品に許可されているビタミン B6 の 1 日の最大推奨摂取量に変更を加えています。現在、ヒト用医薬品のビタミン B6 は、以下の場合を除き、スケジュール 4(処方箋のみ)医薬品での使用に制限されています。
- 医薬品ラベルに関する必須アドバイスステートメント(RASML*)の要件に準拠している場合、推奨される1日用量あたり200 mg以下で50 mgを超えるピリドキシン、ピリドキサール、またはピリドキサミンを含む経口製剤の場合、または
- 推奨される1日量あたり50 mg以下のピリドキシン、ピリドキサール、またはピリドキサミンを含む経口製剤。
*注: RASML では、ラベルに「警告 – チクチク感、灼熱感、またはしびれを感じた場合は、この薬の服用を中止し、できるだけ早く医療従事者にご相談ください。[ビタミン B6 が含まれています]」という (VITB6SX) 文言を記載することが義務付けられています。明確に言えば、推奨される 1 日の摂取量あたり 50 mg 以下のビタミン B6 を含む製品には、ラベルの警告は必要ありません。
ビタミン B6 サプリメントの長期使用に関連する有害事象の検討の結果、オーストラリアとニュージーランドのビタミン B6 の栄養基準値は成人では 1 日あたり 50 mg ピリドキシン、乳児ではそれよりはるかに低く設定されていることから、TGA は許容成分決定の項目を次のように修正することを決定しました。
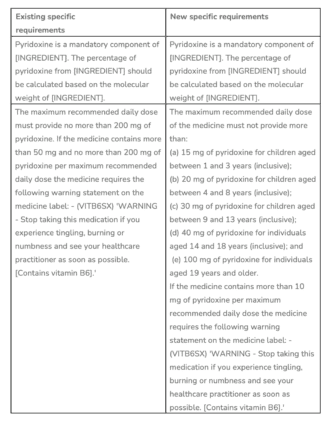
「成分」 = ピリドキサール 5-リン酸、ピリドキサール 5-リン酸一水和物、ピリドキシン塩酸塩。これらは、記載されている医薬品に許可されている形態です。
最終的な変更は 2022 年 3 月 1 日に開始され、スポンサー (MA 保有者) が製品のコンプライアンスを確保できるようにするための 1 年間の移行期間は 2023 年 3 月 1 日に終了します。
オーストラリアの規制変更について詳しく知りたい場合は、RegASK にお問い合わせください。
詳細についてはRegASKにお問い合わせください 続きを読む
