Este artículo se basa en información generada por RegGenius, RegASK AI-impulsado herramienta de inteligencia regulatoria.
En Abril de 2023Dinamarca se convirtió en el primer país europeo en prohibir oficialmente la ashwagandha, exigiendo de inmediato la retirada de todos los productos que contienen esta popular hierba adaptogénica de los estantes de las tiendas. Esta no fue una simple actualización regulatoria rutinaria. En cuestión de meses, lo que comenzó como una decisión de un solo país desencadenaría un efecto dominó en todo el mundo. Europa, obligando a las empresas de suplementos a repensar por completo sus estrategias.
Entre 2023 y 2025, las autoridades se centraron no solo en la ashwagandha, sino también en el kratom, el Tongkat Ali y los extractos de té verde, lo que refleja una mayor preocupación por la seguridad y normas más estrictas de protección del consumidor. Para empresas basadas en hierbas adaptogénicas. [1] y los productos botánicos tradicionales, comprender estos cambios regulatorios no es sólo inteligencia de negocios: es una estrategia de supervivencia.
Este blog examina el panorama regulatorio actual de los suplementos a base de hierbas, explora qué productos botánicos están en riesgo y proporciona estrategias prácticas para mantener el cumplimiento en un mercado global cada vez más complejo.
Lo esencial
- Europa está imponiendo prohibiciones y restricciones a suplementos herbales como ashwagandha, kratom y extractos de té verde debido a preocupaciones de seguridad.
- Las empresas de suplementos de salud se enfrentan a retiros de productos, costos de reformulación y desafíos de cumplimiento complejos en diferentes mercados.
- Los expertos de la industria enfatizan la necesidad de inteligencia regulatoria proactiva, formulaciones diversificadas y documentación de seguridad sólida para mantener el cumplimiento.
Tabla de contenido
- ¿Qué suplementos herbales están bajo mayor escrutinio y por qué?
- El caso de la ashwagandha: la respuesta fragmentada de Europa
- Cómo afectan estas prohibiciones a las empresas de suplementos
- ¿Qué medidas puede tomar para cumplir con la normativa?
- Qué esperar más allá de 2025
- Cómo RegASK ayuda a navegar la complejidad regulatoria global
¿Qué suplementos herbales están bajo mayor escrutinio y por qué?
La industria de los suplementos herbales se enfrenta a una presión regulatoria sin precedentes a medida que las autoridades de todo el mundo intensifican la supervisión de los productos que pueden suponer riesgos para la seguridad. Este escrutinio abarca múltiples cuestiones, desde productos botánicos tradicionales hasta productos contaminados con ingredientes farmacéuticos no declarados. Comprender qué suplementos están bajo revisión regulatoria es crucial para fabricantes, distribuidores y consumidores que navegan por este panorama en constante evolución.
1. Productos botánicos bajo revisión regulatoria en la UE
En la UE, se están revisando varios productos botánicos para determinar su clasificación, seguridad y uso permitido en complementos alimenticios:
- Ashwagandha (Withania somnifera)
- Melatonina
- Kratom (Mitragyna speciosa)
- Algunos productos de la Medicina Tradicional China (MTC)
2. Suplementos para la menopausia bajo la lupa regulatoria
Muchas mujeres recurren a suplementos herbales para controlar los síntomas de la menopausia. Los siguientes ingredientes, que están bajo escrutinio, se encuentran comúnmente en los suplementos para la menopausia:
- Baya del árbol casto (Vitex agnus-castus)
- Trébol rojo (Trifolium pratense)
- Cimicífuga negra (Actaea racemosa)
- Dong quai (Angelica sinensis)
- Maca (Lepidium meyenii)
Los expertos han expresado su preocupación por su seguridad, eficacia, potencial daño hepático e interacciones negativas con otros medicamentos.. Como resultado, yoaumentado Se espera que estos productos estén sujetos a supervisión regulatoria y a un creciente escepticismo por parte de los consumidores.
3. Suplementos que contienen ingredientes prohibidos
Las autoridades reguladoras, como la Autoridad de Ciencias de la Salud de Singapur (HSA)), Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) y Salud Canadá, han emitido múltiples avisos sobre suplementos herbales y de salud que contienen ingredientes no declarados o prohibidos, entre ellos: [2] [3]
- Esteroides (por ejemplo, dexametasona, prednisolona)
- Sibutramina (fármaco prohibido para bajar de peso)
- Inhibidores de la fosfodiesterasa tipo 5 (PDE-5) (p. ej., sildenafil, tadalafil)
- Diclofenaco
- Hidroquinona
- Fluoxetina
- Prasterona (DHEA)
- Metocarbamol
- Lidocaína
- fenolftaleína
- Senósidos
Estos ingredientes se han relacionado con efectos adversos graves, como eventos cardiovasculares, daño hepático, trastornos renales y otros riesgos para la salud. Los productos que contienen estas sustancias están sujetos a retiradas del mercado, prohibiciones y medidas de control. Dichos productos representan riesgos significativos para la salud debido a ingredientes no divulgados y posibles interacciones farmacológicas.
4. Suplementos adulterados con No declarado productos farmacéuticos
Los reguladores globales están tomando medidas enérgicas contra los suplementos que contienen ingredientes farmacéuticos no declarados, que a menudo se disfrazan de productos “naturales” para la mejora sexual, la pérdida de peso o la energía. Ministerio de Salud de Israel Ha emitido advertencias sobre sustancias ocultas como sildenafil, tadalafilo, y levodopa, lo que puede provocar graves riesgos para la salud si se toma sin saberlo.
5. Suplementos contaminados y falsificados
Más allá de las drogas ocultas, los suplementos contaminados con metales pesados, toxinas microbianas, o que se venden como falsificaciones siguen siendo una importante preocupación mundial. Los organismos reguladores están intensificando las pruebas de productos y los controles de importación para proteger a los consumidores y sancionar a las marcas que no cumplen con las normas.
El caso de la ashwagandha: la respuesta fragmentada de Europa
La ashwagandha (Withania somnifera) se ha convertido en uno de los productos botánicos más controvertidos en el mercado europeo de suplementos. Impulsado por el interés de los consumidores por el alivio del estrés y la salud natural, el volumen del mercado europeo de ashwagandha aumentó en 10,91 TP18T entre 2019 y 2022, con una previsión de crecimiento continuo de dos dígitos hasta 2030. [5]
¿Por qué la ashwagandha se convirtió en un objetivo regulatorio?
La popularidad de Ashwagandha resultó ser su perdición. A medida que millones de personas recurrían a la ashwagandha para aliviar el estrés y controlar la ansiedad, los organismos reguladores comenzaron a preocuparse por su complejo perfil químico. A diferencia de los medicamentos monomoleculares, el extracto de raíz de ashwagandha contiene docenas de compuestos activos, incluyendo withanólidos, lo que dificulta la evaluación de su seguridad. El punto de inflexión regulatorio se produjo cuando surgieron informes de eventos adversos, en particular casos de toxicidad hepática. Si bien la mayoría se relacionaban con productos contaminados o dosis extremas, el daño ya estaba hecho, y los reguladores europeos actuaron.
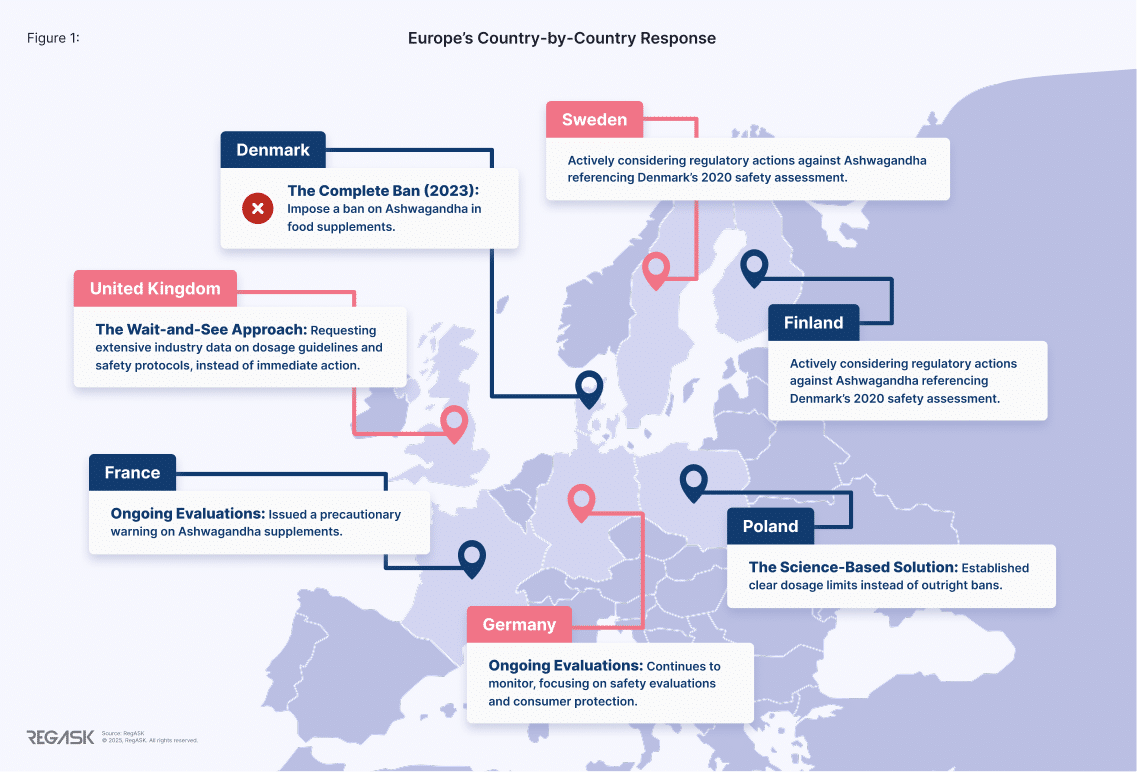
La respuesta de Europa país por paísmi
Dinamarca: La prohibición total (2023)
Dinamarca se convirtió en el primer país de la UE en imponer una prohibición de la ashwagandha en los complementos alimenticios, tras una evaluación de riesgos de 2020 realizada por la Universidad Técnica de Dinamarca (DTU) que planteó preocupaciones sobre la alteración hormonal y los posibles riesgos reproductivos. [6] [7]
La Administración Danesa de Veterinaria y Alimentos (DVFA) aplicó la prohibición rápidamente, exigiendo la retirada de los productos del mercado. Esta decisión tuvo un gran impacto en las empresas de suplementos que operan en la región nórdica, con grupos del sector. reportando pérdidas financieras significativas.[8]
Reino Unido: la estrategia de esperar y ver
La Agencia de Normas Alimentarias del Reino Unido optó por una revisión exhaustiva en lugar de una acción inmediata, solicitando a la industria datos exhaustivos sobre las pautas de dosificación y los protocolos de seguridad. Si bien fue más mesurada, esto creó un limbo regulatorio para los fabricantes, quienes no pudieron tomar decisiones a largo plazo.
Polonia: La solución basada en la ciencia
Polonia estableció límites de dosis claros en lugar de prohibiciones absolutas:
- Polvo de raíz de ashwagandha: máximo 3 g al día [9]
- Extractos estandarizados: Máximo 10 mg diarios [10]
Alianza Nórdica: Suecia y Finlandia
Suecia y Finlandia están considerando activamente acciones regulatorias contra la ashwagandha, haciendo referencia principalmente a la evaluación de seguridad de 2020 realizada por la Universidad Técnica de Dinamarca (DTU) como justificación.
Francia y Alemania: evaluaciones en curso [11] [12]
En 2024, la agencia francesa de seguridad alimentaria, ANSES, emitió una advertencia preventiva sobre los suplementos de ashwagandha, recomendando a los grupos vulnerables —incluidas las mujeres embarazadas o en período de lactancia, los menores de edad y las personas con afecciones tiroideas, hepáticas o cardíacas— evitar su uso debido a los efectos adversos notificados y a la escasez de datos de seguridad. Esto ha dado lugar a requisitos de etiquetado más estrictos y a una mayor supervisión regulatoria en el mercado francés de suplementos para la salud.
Mientras tanto, Alemania continúa monitoreando los suplementos herbales como la ashwagandha a través de su Instituto Federal de Evaluación de Riesgos (BfR), concentrándose en evaluaciones de seguridad y protección del consumidor, aunque no se han promulgado prohibiciones formales.
Cómo afectan estas prohibiciones a las empresas de suplementos
Impacto financiero en toda la cadena de suministro
La incertidumbre regulatoria en torno a la ashwagandha interrumpió la cadena de suministro en múltiples niveles. Los proveedores de materias primas sufrieron una fuerte caída de pedidos, especialmente en los mercados con restricciones.
Los fabricantes por contrato se vieron obligados a reformular productos, lo que a menudo les generó altos costos para encontrar alternativas, revalidar fórmulas y actualizar las etiquetas. En algunos casos, las empresas tuvieron que gestionar retiradas de productos o afrontar desabastecimientos debido a la interrupción de la distribución. Estos desafíos ponen de relieve la necesidad crucial de que las empresas supervisen de cerca el entorno regulatorio y desarrollen estrategias con visión de futuro para proteger la continuidad del negocio y minimizar el riesgo financiero. [6] [7] [9]
La pesadilla del cumplimiento
Gestionar la regulación de la ashwagandha en múltiples mercados europeos se ha convertido en un desafío constante para las empresas de suplementos. Actualmente, las empresas suelen necesitar diferentes formulaciones y etiquetas. Según informa NutraIngredients. [10]Los líderes de la industria describen la complejidad de navegar entre regulaciones nacionales divergentes como “una pesadilla logística”, y algunas empresas se ven obligadas a gestionar múltiples versiones de productos para diferentes mercados.
Un ejecutivo de asuntos regulatorios de una empresa líder en suplementos explicó: «Pasamos de gestionar una fórmula europea a gestionar ocho versiones diferentes. Tan solo la complejidad casi destrozó a nuestro equipo de operaciones».
(Entrevista de la industria, 2025)
Confianza en la marca y confusión del consumidor
Quizás lo más perjudicial fue el impacto en la confianza del consumidor. Los compradores acostumbrados a comprar ashwagandha en línea se encontraron repentinamente con información contradictoria sobre su seguridad. Las redes sociales se llenaron de clientes confundidos que preguntaban: "¿Es segura la ashwagandha?" y "¿Por qué está prohibida?".
Las empresas invirtieron fuertemente en la educación del consumidor, explicándole la diferencia entre el extracto de ashwagandha de calidad estandarizada y los productos potencialmente problemáticos. Quienes contaban con ashwagandha verificada por la USP y con productos certificados por la NSF obtuvieron una ventaja competitiva.
¿Qué medidas puede tomar para cumplir con la normativa?
1. Crear documentación a prueba de balas: Guías RegASK
En un clima de creciente escrutinio regulatorio, la documentación no es solo una formalidad; es la primera línea de defensa. Las empresas más resilientes van más allá de recopilar estudios existentes; desarrollan expedientes estratégicos que anticipan las preocupaciones regulatorias.
Guías RegASK Valida con pericia paquetes de seguridad y cumplimiento diseñados para cumplir con los estándares globales. Ya sea que se trate de riesgos toxicológicos, umbrales de dosificación o restricciones de uso, estas guías están diseñadas para anticipar objeciones, no para reaccionar ante ellas.
2. Aprovechar la inteligencia regulatoria proactiva
Esperar a que aparezca una prohibición en una publicación especializada ya no es una estrategia viable. Las empresas que se adelantaron a la tendencia utilizaron Inteligencia regulatoria impulsada por IA para monitorear los riesgos globales emergentes en tiempo real.
El uso de soluciones como RegASK ayuda a identificar cambios en la percepción regulatoria antes de que se implementen restricciones formales. Esto brinda tiempo para explorar ajustes en la formulación y el etiquetado, adaptar las estrategias de mercado o interactuar con los reguladores de forma temprana. Esta previsión ayuda a las empresas a mantener el acceso a mercados clave y a aprovechar oportunidades en regiones con un entorno regulatorio más favorable.
Ser proactivo no solo garantiza el cumplimiento; también lo desbloquea. ventajas competitivas de tiempo en entornos regulatorios cada vez más fragmentados.
3. Adoptar estrategias de diversificación de ingredientes
Depender excesivamente de un solo ingrediente estrella puede convertirse rápidamente en un problema. Cuando ingredientes como la ashwagandha se enfrentaron a prohibiciones o límites estrictos de dosis, las empresas que habían diversificado sus fórmulas lograron adaptarse, mientras que las marcas monoingrediente se vieron en apuros.
Equipos con visión de futuro combinan ashwagandha con rodiola, magnesio u otros adaptógenos para desarrollar fórmulas que no solo sean efectivas sino también resistentes a las regulaciones. La inteligencia regulatoria de RegASK puede guiarlo en la identificación de alternativas de ingredientes que cumplan con las normas Adaptado a su mercado y categoría.
La diversificación de ingredientes no es sólo una red de seguridad; es una estrategia de innovación de productos impulsada por la previsión regulatoria.
Qué esperar más allá de 2025
A medida que se intensifica el escrutinio global sobre los suplementos herbales, las empresas deben prepararse para un futuro regulatorio más estructurado y basado en datos. Tres tendencias clave definirán el panorama posterior a 2025.
La armonización global se está acelerando. Si bien las regulaciones botánicas siguen estando fragmentadas hoy en día, iniciativas como la Estrategia de medicina tradicional de la OMS [13] Señalan un cambio hacia estándares de seguridad unificados. Para las marcas globales, la complejidad a corto plazo persiste, pero se está abriendo camino hacia un cumplimiento simplificado.
El cumplimiento impulsado por IA se está convirtiendo en la norma de la industria. Los equipos reguladores modernos están recurriendo a soluciones como RegASK para anticipar cambios, mapear los riesgos de los ingredientes y agilizar los flujos de trabajo para ayudar a eliminar las conjeturas del cumplimiento global.
Se requieren afirmaciones basadas en evidencia. Las autoridades están endureciendo las restricciones sobre las afirmaciones de salud sin fundamento. El éxito dependerá de la validación clínica, la transparencia y la capacidad de adaptarse rápidamente a los nuevos requisitos de justificación de las afirmaciones. Comprender las regulaciones y procesos locales.
De cara al futuro, el cumplimiento normativo no se trata solo de mantenerse al día, sino de mantenerse a la vanguardia. Los ganadores serán quienes consideren la agilidad regulatoria como una estrategia empresarial fundamental.
Cómo RegASK ayuda a navegar Complejidad regulatoria global
RegASK simplifica la toma de decisiones regulatorias con una solución basada en IA que ofrece información oportuna, documentación inteligente y orquestación del flujo de trabajo. Desde la identificación de factores de riesgo hasta la gestión del cumplimiento normativo en todas las regiones, RegASK permite a los equipos regulatorios actuar con mayor rapidez, mitigar los riesgos a tiempo y anticiparse a los cambios, a nivel global y a gran escala.
¿Está listo para preparar su estrategia de cumplimiento para el futuro? Reservar una demostración para ver cómo RegASK puede ayudarlo a navegar la complejidad regulatoria con confianza.
Preguntas frecuentes (FAQ)
- ¿Por qué Dinamarca prohibió la Ashwagandha? Dinamarca prohibió la ashwagandha en 2023 después de que una evaluación de riesgos revelara posibles alteraciones hormonales y problemas de seguridad reproductiva. La Administración Veterinaria y Alimentaria danesa exigió la retirada del mercado de todos los productos que contienen ashwagandha para proteger la salud pública.
- ¿Qué otros suplementos herbales se enfrentan a un mayor escrutinio en Europa? Además de la ashwagandha, varios suplementos herbales se encuentran bajo revisión regulatoria en Europa, incluyendo el kratom, los extractos de té verde, el sauzgatillo, el trébol rojo, la cimicífuga negra y el dong quai. Las autoridades están evaluando su seguridad, su posible toxicidad hepática y... posibles interacciones con medicamentos, lo que puede dar lugar a regulaciones o prohibiciones más estrictas.
- ¿Cómo afectan estas prohibiciones a las empresas globales de suplementos? Las prohibiciones globales generan importantes desafíos operativos, como retiradas de productos, costos de reformulación, requisitos de cumplimiento específicos de cada país y pérdida de confianza del consumidor. Muchas empresas están adoptando plataformas de inteligencia regulatoria para monitorear y gestionar proactivamente estos riesgos.
- ¿Cómo pueden las empresas prepararse para el futuro frente a los cambios en las regulaciones sobre los suplementos herbales? Las empresas deberían invertir en documentación de seguridad integral, inteligencia regulatoria basada en IA, carteras de ingredientes diversificadas e investigación clínica basada en la evidencia. Plataformas como RegASK Ayudar a las empresas a anticipar los cambios regulatorios y mantener el acceso al mercado a nivel mundial.
Referencias y citas
- sciencedirect.com – Adaptógeno
- hsa.gov.sg – Información actualizada de la HSA sobre productos encontrados en el extranjero que contienen ingredientes potentes (marzo de 2025)
- hsa.gov.sg – Alerta de la HSA: Se encontraron cuatro productos con potentes ingredientes medicinales, incluyendo esteroides y una sustancia prohibida. Cuatro consumidores experimentaron efectos adversos tras consumir tres de estos productos.
- gov.il – Productos “naturales” falsificados
- kbvresearch.com – mercado europeo del extracto de ashwagandha
- pmc.ncbi.nlm.nih.gov – Prohibición danesa de la ashwagandha: verdad, evidencia, ética y regulaciones
- mcgill.ca – ¿Por qué Dinamarca prohibió la Ashwagandha?
- olemiss.edu – ashwagandha-khan-chittiboyina
- vitafoodsinsights.com – Actualización regulatoria de la UE sobre la ashwagandha
- nutraingredients.com – Crece la preocupación por la seguridad de la ashwagandha en los estados miembros de la UE.
- foodcomplianceinternational – Francia emite una opinión sobre los posibles efectos adversos de la ashwagandha
- .bfr.bund.de – Ashwagandha: suplementos alimenticios con posibles riesgos para la salud
- mtci.bvsalud.org – La OMS convoca la primera cumbre mundial de alto nivel sobre medicina tradicional para explorar la base de evidencia y las oportunidades para acelerar la salud para todos.