この記事は元々 DIA Global発行の「Global Forum」誌、2026年5月号。.
元の記事はこちらからお読みください。 DIA グローバル フォーラム – 2026 年 5 月号
毎週、ほぼ半数が 規制関連業務に携わる専門家の多くは、影響評価書の作成、書類の更新、申請決定に至るまでに、規制変更の追跡だけで2~3日を費やしています。これを複数の管轄区域にまたがって考えると、それぞれの管轄区域には独自の用語、規則、執行方針があり、計算が合わなくなります。複雑さの増大に人員を増やすことは不可能です。.
しかし、解決策は、生成型AIを既存のワークフローに単純に重ね合わせることではありません。生成型AIは要約や草稿作成はできますが、調整することはできません。RAチームが必要としているのは、変更を検知し、その影響を分析し、対応策を草稿し、承認のために送付し、すべてのステップを、管理された範囲内で自律的にログに記録するシステムです。そのようなシステムがエージェント型AIであり、早期導入企業はすでにその有効性を証明しています。エージェント型AIは、規制情報、申請、品質管理システム(QMS)、および医薬品安全性監視(PV)ワークフローを、単一の調整されたシステムとして運用することを可能にし、資格を有する規制関連担当者、品質保証担当者、および資格を有する担当者(QP)が、すべての段階で完全な意思決定権限と責任を保持します。.
基盤となる層:規制業務の近代化におけるGenAIの役割
規制の複雑化が指数関数的に増大している現状では、従来のデジタルツールだけでは不十分であり、規制関連業務(RA)機能の根本的な再構築が求められている。.
によると 2025年デロイト調査, ライフサイエンス分野の経営幹部の大多数は、規制の複雑さを上位3つの業務リスクの1つとして挙げている。規制関連チーム全体で、業務量は依然として膨大であり、プロセスは依然として手作業に大きく依存している。. 過去2年間の調査 専門家の約451,180万人が、規制変更の監視だけで毎週2~3日を費やしていることが明らかになった。これは、要求事項の変化、多言語対応、そして絶え間ない複雑さによって、さらに時間のかかる作業となっている。その結果、リソースの逼迫、意思決定の遅延、そして市場機会の逸失につながっている。.
規制の複雑さが重大な転換点に達し、 EU 人工知能 (AI) 法 規制当局のガイドラインが世界的に拡大する中、RAチームは明確な選択を迫られています。手動によるモニタリングを継続するか、AIを活用したインテリジェンスを採用するかです。このような状況下で、, 生成AI(GenAI), 大規模なデータセットからコンテンツを生成、要約、または再構成できる高度な機械学習モデルは、今や不可欠な機能となっています。これにより、情報収集が自動化され、新たなトレンドが明らかになってリスクを未然に防ぎ、文書レビューが効率化されます。.
規制関連業務における主な応用例は以下のとおりです。
- 自動文書要約
- 長文の規制に関する最新情報やガイダンスを、社内チーム向けの簡潔な情報レポートに変換する。.
- 標準作業手順書(SOP)、申請書類、トレーニングコンテンツの初期草案を作成することで、規制関連チームの反復的な文書作成作業を大幅に削減します。.
- 予測コンプライアンス監視
- 過去のデータとリアルタイムデータを用いて、規制リスク、検査準備状況、および表示変更を予測する。.
- 高度な大規模言語モデルを活用することで、複雑な規制文書を迅速に分析・要約し、的を絞った質問に回答し、管轄区域間の要件を比較することで、時間のかかる手作業によるレビューを排除します。.
- 品質管理システム(QMS)におけるAI
- 文書作成および精緻化、逸脱管理、医薬品安全性監視報告を支援する。.
- 社内規定を新規または更新された規制に照らし合わせて評価し、矛盾点を特定し、さらにはギャップを埋めるための是正措置を提案する。.
- グローバル貿易およびサプライチェーンコンプライアンス
- 要件の解釈など FDAの固有医療機器識別子 (UDI)と EUDAMED, そして、地域間で表示基準を統一すること。.
- 多言語コンプライアンスのサポート:言語モデルは、グローバルな事業運営に不可欠な法的トーンと文脈を維持しながら、規制コンテンツをさまざまな市場向けに翻訳および適応させることができます。.
- ガバナンスと人的監督
- コントロールを埋め込んで、 EU AI法 また、リスクベースのガバナンスと説明責任を義務付けるその他のグローバルな枠組みも含まれる。.
- 規制結果を予測する
- グローバルな規制情報源を継続的に監視し、変更を検知してタイムリーなアラートを発信することで、チームが進化する要件に常に先んじて対応できるようにします。.
- 過去の承認傾向を分析することにより、, AIは潜在的な意思決定を予測し、リスクの高い領域を特定することができる。, これにより、積極的な計画策定と資源配分が可能になります。.
しかし、GenAIだけでは最終目標にはなり得ません。GenAIは貴重な洞察を提供しますが、現代の規制関連業務を特徴づける複雑な多段階ワークフローを単独で実行することはできません。洞察をコンプライアンスに準拠した行動へと一貫して転換するには、組織はエージェント型AIへと移行する必要があります。エージェント型AIでは、ソフトウェアエージェントが人間の監視下でワークフローを計画、実行、適応させます。.
GenAIが触媒となる場合、エージェント型AIは統合制御アーキテクチャとして機能し、検出、分析、作成、通知、監査証跡を単一の自動化された運用チェーンにリンクさせる。.
エージェントの飛躍:プロアクティブな洞察からワークフローオーケストレーションへ
エージェントAI エージェント型AIとは、定義されたパラメーター内で動作し、接続されたシステム全体にわたって認識、推論、および行動を行うことができる、目標指向型のソフトウェアエージェントを指します。プロンプトに応答する汎用AIとは異なり、エージェント型AIはワークフローを体系的に調整し、事前に定義された目標を達成します。これは、受動的な自動化から能動的な実行への根本的な転換を意味します。.
この進化は遠い未来の話ではなく、まさに今起こっていることです。エージェント型AIを導入した組織は、既に規制リスクの低減、監査対応能力の向上、市場参入の加速を実現しています。以下の実例パイロットプロジェクトは、その具体的な効果を示しています。.
規制関連業務におけるエージェント型AIパイロット:理論から実践へ
以下のパイロットケーススタディは、文書化された業界動向とAI駆動型規制ワークフローに関する公開された知見に基づいた例示です。これらは、主要な情報源によって報告された共通のテーマを反映しています。 生命科学におけるエージェント型AI, 議論について 書類自動化、 そして 規制業務のためのマルチエージェントアーキテクチャ. これらの事例は、業界レポートやオピニオン記事で紹介されている実際の導入事例から得られた、処理時間の短縮、精度の向上、ガバナンスの強化といったメリットをまとめたものです。また、ターゲットを絞ったエージェント型AIの導入が、いかに測定可能な成果をもたらしているかを示しています。.
パイロットA: グローバルなラベル表示変更のオーケストレーション
- ビジネスケース:中規模の製薬会社は、25の市場におけるラベル変更の影響評価に平均10日間を要し、その結果、12%の割合で更新漏れが発生していた。.
- 解決策:保健当局のウェブサイトを監視し、表示関連の更新を特定し、会社の製品ポートフォリオに対する初期影響分析を実行し、人間によるレビューのための影響メモを作成するために、エージェント型AIワークフローが導入されました。.
- 安全対策:役割に基づくアクセス制御、情報源の追跡、および機械翻訳されたすべてのコンテンツに対する必須の二言語レビュー。.
- 主要な規制/品質フレームワーク:このパイロットプロジェクトは、いくつかの主要な規制および品質フレームワークの交点において実施されました。
- ICH Q9(R1) ステップ4文書品質リスク管理(2023年1月採択):品質リスク管理プロセスにおけるAI由来のリスクスコアとコントロールの使用を規定し、客観性、主観性の最小化、リスクに基づく意思決定に関する要件を含みます。このパイロットプロジェクトにおけるAI影響スコアリングロジックは、4つの主要な改善領域に沿って設計されました。.
- EU MDR(規則(EU)2017/745)/ EU IVDR(規則(EU)2017/746)+ MDCG 2025-6:影響を受ける製品ポートフォリオに医療機器または体外診断用医薬品が含まれる場合、表示変更とその影響評価は、技術文書、使用説明書(IFU)、および市販後監視に関するMDR/IVDRの義務の対象となります。2025年6月のMDCGガイダンスでは、AI支援表示レビューツールは、MDR/IVDRとEU AI法の二重の枠組みの下で透明性と人間の監視の要件を満たす必要があることが明確化されました。.
- FDAのラベル表示ガイダンスとPCCP:米国市場向け製品の場合、AI支援によるラベル表示変更ワークフローは、FDAの事前決定変更管理計画(PCCP)フレームワークによって管理されます。このフレームワークでは、AIによる機器ラベル表示の変更はすべて文書化され、追跡可能であり、ユーザーに通知されることが求められます。パイロット版のバージョン管理とメモ作成の出力は、PCCPの開示要件と互換性があるように構成されました。参照: FDA PCCPガイダンス.
- 結果(6ヶ月間の試験運用):
- メモが反映されるまでの平均時間が40%短縮されました(10日から6日)。.
- 更新漏れはほぼゼロにまで減少しました(<1%)。.
- 下流工程におけるバージョン管理エラーは50%減少しました。.
パイロットB: モジュール1の書類作成の自動化
- ビジネスケース:あるジェネリック医薬品会社は、提出用のモジュール1ドシエ(地域別フォーム、カバーレターなど)の作成に大幅な遅延が生じ、再作業サイクルにチームの時間の30%以上が費やされました。.
- 解決策:エージェントを訓練し、社内システムからのデータを使用して国別のテンプレートに自動的に入力し、必要なPDF文書を組み立て、電子提出(RPS/eCTD)用にパッケージ化しました。.
- 安全対策:厳格なテンプレート検証、最終化前の必須の人的承認、および非標準要件のための例外キュー。結果(9ヶ月間のパイロット運用):
- モジュール1の組み立てサイクル時間は35%~45%短縮されました。.
- 事務処理上のミスによる手戻り作業は、30%によって削減された。.
規制運用モデルの次なる進化:AIによる積極的な実行
エージェントとは、独立して行動し、選択を行い、自分の行動を制御する能力を指します。エージェントAIはこの概念をデジタル領域に持ち込みます。規制科学は、これが実際に何を意味するのかを形式化し始めています。 FDA–EMA 医薬品開発における優れたAI実践のための指針 (2026年1月)AIシステムを定義する OECD 「展開後に適応性を示す可能性のある、さまざまなレベルの自律性で動作するように設計された機械ベースのシステム」という定義は、エージェントアーキテクチャを直接包含する。 EU AI法 さらに、自律型AIシステムをリスクレベルに応じて分類し、透明性、人間の監視、ライフサイクルガバナンスに関して相応の義務を課すことで、これをより具体的に運用する。. ISO/IEC 42001:2023, 初の国際AI管理システム標準である は、AIリスク評価、影響評価、継続的改善を網羅する組織ガバナンスの枠組みを提供し、その中でエージェントの展開を構造化する必要があります。その目標指向の機能は、組織に代わって行動する権限を与えられています。, 定義済みで人間が承認したパラメータに基づいてアクションを実行する.
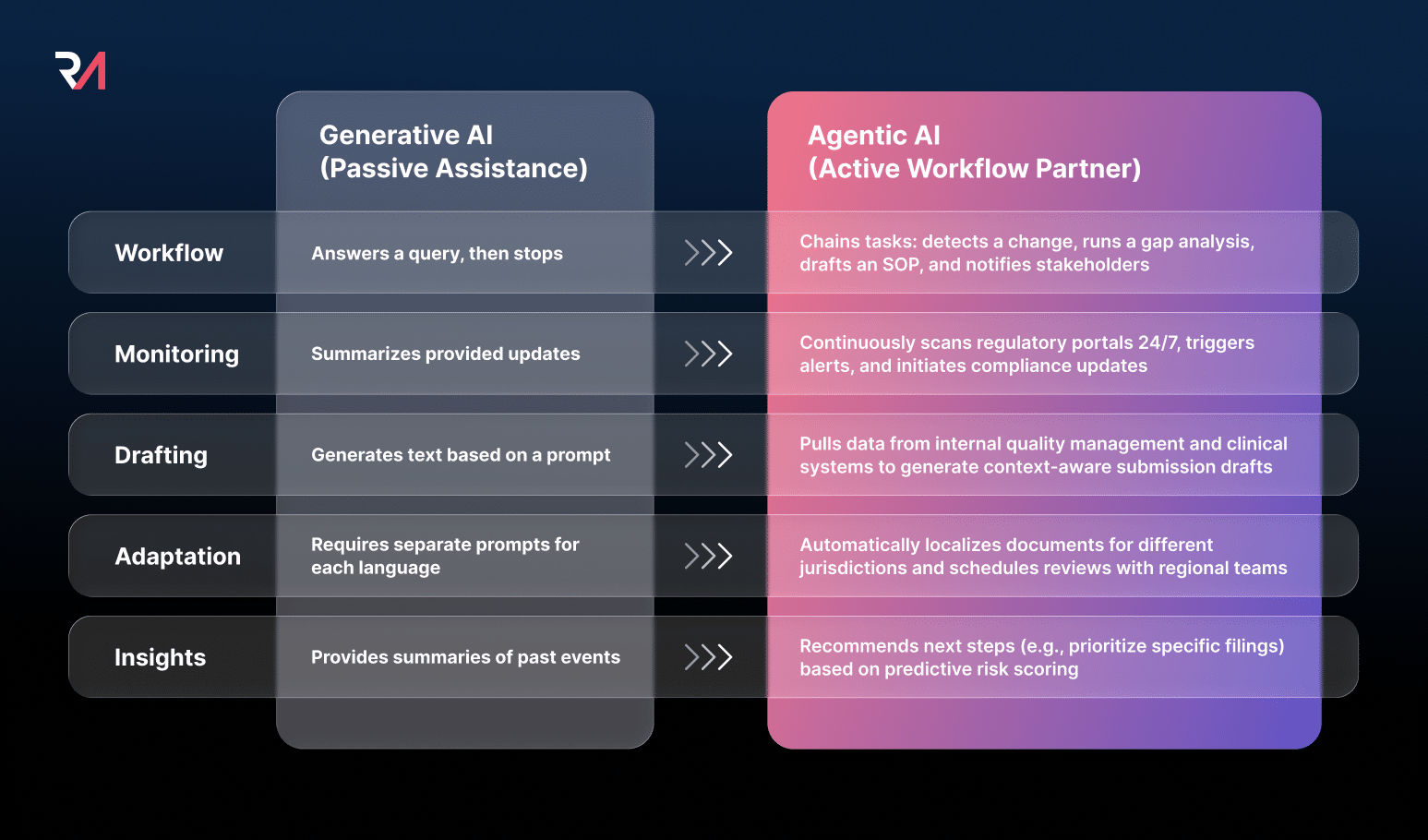
エージェント型AIは、受動的な自動化を超え、定義され統制された境界内でタスクの計画、実行、適応を行います。以下に、エージェント型AIが上記の機能を向上させるいくつかの方法を示します。
- 動的ワークフローオーケストレーション: クエリに答えるだけでなく、エージェント型AIはタスクを連鎖させることができます。新しい規制の検出 → ギャップ分析の実行 → 更新されたSOPの草案作成 → 関係者への通知。規制対象の出力(SOP、提出文書、ラベル)に触れる連鎖型エージェントワークフローは、GxPコンピュータシステム検証の対象となります(参照: GAMP 5 | GAMP AIガイド) エージェントが作成または変更したSOPまたは提出文書は、規制対象の電子記録を構成し、 FDA 21 CFR Part 11 (米国) そして EU GMP附属書11 (EU)の要件。.
- 継続的な監視と積極的な対応: 規制ポータルを継続的にスキャンし、アラートをトリガーし、手動の指示を待たずにコンプライアンスの更新を開始することもできます。コンプライアンスの決定に反映される自律的な規制監視は、まさにその範囲内にあります。 ICH Q9(R1) 品質リスク管理。.
- コンテキスト認識型ドラフト作成:エージェント型AIは、複数の内部システム(臨床試験データベース、品質システムなど)からデータを取得し、カスタマイズされた提出用ドラフトを生成できます。エージェント型AIが臨床試験データベースにアクセスして提出用コンテンツを生成する場合、複数の重複するフレームワークの下で同時に動作します。 ICH M8/eCTD v4.0, 電子提出を目的とするあらゆるコンテンツの構造、メタデータ、およびトレーサビリティ要件を管理するため。 EMAのAIに関する考察論文 製品情報や提出文書の作成に使用される生成言語モデルは、厳密な人間の監視下で使用され、規制当局への提出前に事実と構文の正確性を保証する品質レビューメカニズムが設けられなければならないことが明示されています。臨床データや患者レベルのデータにアクセスする場合、, GDPR (規則(EU)2016/679)および同等のデータ保護制度は、データ最小化、目的制限、およびアクセス管理の義務を課しています。.
- 多言語対応と市場固有の適応:異なる管轄区域向けに文書を自動的にローカライズし、地域チームとのレビューをスケジュールできます。. GAMP 5 検証要件は、GxP準拠のコンピュータシステムとして、ローカライズ剤自体にも適用されます。.
- 予測的および処方的洞察: 予測を超えて、エージェント型 AI はリスク スコアリングに基づいて次のステップ (特定の申請の優先順位付け、リソースの割り当てなど) を推奨できます。AI が生成したリスク スコアと推奨事項が、提出の優先順位付け、コンプライアンス タイムラインに対するリソースの割り当て、医薬品安全性監視のエスカレーションのシグナルなど、規制上の決定に影響を与える場合、, ICH Q9(R1) は主要な品質フレームワークです。 FDAとEMAによるAI(人工授精)に関する優良実施基準の共同原則 医薬品開発においては、原則2(リスクベースのアプローチ)と原則8(ライフサイクル管理)を通じてこれを強化しており、検証、監視、および安全対策のレベルは、AIの使用状況と関連するリスクに合致していなければならないと述べている。.
これは単なる自動化ではなく、効率性と戦略的価値への根本的な転換である。.
上記で述べた効率性と戦略的利益は、組織がすべてのエージェント型AI導入の最初から設計に組み込まなければならない、譲ることのできない制約の範囲内で機能する。
- AIエージェントは、規制や科学的な業務を支援するために使用されるものであり、正式な判断や説明責任に取って代わるものではありません。.
- 標準作業手順書、ラベル表示、提出書類など、AIが生成したすべての出力は、保健当局と共有される前に、文書化された人間のレビューと承認の対象となります。.
- 承認の可能性の評価や保健当局の予想される措置など、エージェント型AIによって生成される予測分析は、意思決定支援のみを目的としており、確定的な予測や規制当局が承認した予測とはみなされません。.
規制当局のリーダーは、企業全体の変革を待つ必要はありません。まずは、ホライズンスキャニング、ドシエ作成、ラベル変更監視など、処理量が多く反復的なワークフローを特定し、単一の製品ラインまたは市場クラスター内でエージェント型アプローチを試験的に導入することから始めましょう。アクションまでの時間、更新漏れ率、戦略的な業務に再配分されたチーム時間など、明確な指標を用いて90日間の評価期間を設定します。今日、規制運用モデルにエージェント型AIを組み込んだ組織は、複雑性に対応するだけでなく、それを競争優位性へと転換できるでしょう。的を絞った実装は始まりに過ぎません。エージェント型AIを拡張するには、成熟度ロードマップ、マルチエージェントアーキテクチャ、規制環境向けに設計されたガバナンスが必要です。(このシリーズの次の記事では、これら3つすべてを構築する方法について解説します。)
この記事では、 2025年8月 グローバルフォーラム 臨床業務を超えて規制関連業務(RA)機能へのエージェント型AIに関する議論、「“人工知能の次のステップ:エージェント型AI。」

