Cet article a été initialement publié dans le Numéro de mai 2026 du magazine Global Forum de DIA Global.
Lire la publication originale ici : Forum mondial DIA – Numéro de mai 2026
Chaque semaine, près de la moitié En moyenne, les professionnels des affaires réglementaires perdent deux à trois jours à suivre l'évolution de la réglementation avant même la rédaction d'une analyse d'impact, la mise à jour d'un dossier ou la prise d'une décision de dépôt. Multipliez ce temps par plusieurs juridictions, chacune avec son propre langage, son rythme et ses pratiques d'application, et le calcul devient impossible. Les effectifs ne peuvent pas suivre le rythme de la complexité croissante.
Pourtant, la solution ne consiste pas simplement à superposer l'IA générative aux flux de travail existants. L'IA générative peut synthétiser et rédiger des documents, mais elle ne peut pas orchestrer l'ensemble du processus. Les équipes des affaires réglementaires ont besoin d'un système capable de détecter un changement, d'en analyser l'impact, de rédiger la réponse, de la soumettre à l'approbation et de consigner chaque étape, de manière autonome et dans le respect des limites définies. Ce système, c'est l'IA agentive, et les premiers utilisateurs en prouvent déjà l'efficacité. L'IA agentive permet aux flux de travail liés à la veille réglementaire, aux soumissions, aux systèmes de gestion de la qualité (SGQ) et à la pharmacovigilance (PV) de fonctionner comme un système unique et orchestré, où le personnel qualifié en affaires réglementaires, en assurance qualité et les personnes qualifiées (PQ) conservent l'entière autorité décisionnelle et la responsabilité à chaque étape.
La couche fondamentale : le rôle de GenAI dans la modernisation des affaires réglementaires
La croissance exponentielle de la complexité réglementaire exige plus que les outils numériques traditionnels ; elle nécessite une refonte fondamentale de la fonction des affaires réglementaires (AR).
Selon un Enquête Deloitte 2025, La plupart des dirigeants du secteur des sciences de la vie citent la complexité réglementaire comme l'un de leurs trois principaux risques opérationnels. Au sein des équipes des affaires réglementaires, la charge de travail demeure considérable et les processus sont encore largement manuels. Enquêtes menées au cours des deux dernières années Les données indiquent que près de 451 000 professionnels consacrent deux à trois jours par semaine à la seule veille réglementaire, une activité chronophage amplifiée par l’évolution constante des exigences, la multiplicité des langues et la complexité persistante. Il en résulte une surcharge de travail, des prises de décision plus lentes et des opportunités de marché manquées.
Alors que la complexité réglementaire atteint un point d'inflexion critique, avec l'application de la Loi européenne sur l’intelligence artificielle (IA) Avec l’approche et l’expansion mondiale des directives réglementaires, les équipes RA sont confrontées à un choix clair : continuer à surveiller manuellement ou adopter l’intelligence artificielle. Dans ce contexte, Intelligence artificielle générative (GenAI), Les modèles d'apprentissage automatique avancés, capables de générer, de résumer ou de reformuler du contenu à partir de vastes ensembles de données, sont devenus une capacité fondamentale. Ils automatisent la collecte de renseignements, mettent en évidence les tendances émergentes pour anticiper les risques et rationalisent l'examen des documents.
Les principales applications dans le domaine des affaires réglementaires comprennent :
- Résumé automatisé de documents
- Transformer les longs documents réglementaires ou les directives en rapports d'information concis pour les équipes internes.
- Production des premières versions des procédures opérationnelles standard (SOP), des dossiers de soumission et du contenu de formation, réduisant considérablement les tâches de rédaction répétitives pour les équipes réglementaires.
- Surveillance prédictive de la conformité
- Utilisation de données historiques et en temps réel pour prévoir les risques réglementaires, la préparation aux inspections et les modifications d'étiquetage.
- Analyse et synthèse rapides de documents réglementaires complexes, réponses à des questions ciblées et comparaison des exigences entre juridictions, élimination des examens manuels fastidieux grâce à des modèles linguistiques avancés de grande taille.
- L'IA dans les systèmes de gestion de la qualité (SGQ)
- Génération et perfectionnement de la documentation de soutien, gestion des écarts et rapports de pharmacovigilance.
- Évaluer les politiques internes au regard des réglementations nouvelles ou mises à jour, identifier les incohérences et même proposer des mesures correctives pour combler les lacunes.
- Conformité au commerce mondial et à la chaîne d'approvisionnement
- Interpréter les exigences telles que Identifiant unique de dispositif de la FDA (UDI) et EUDAMED, et d'harmoniser les normes d'étiquetage entre les régions.
- Soutien à la conformité multilingue : les modèles linguistiques peuvent traduire et adapter le contenu réglementaire aux différents marchés tout en préservant le ton et le contexte juridiques essentiels aux opérations mondiales.
- Gouvernance et contrôle humain
- Intégration de contrôles pour s'aligner sur Loi européenne sur l'IA et d’autres cadres mondiaux qui imposent une gouvernance fondée sur les risques et l’explicabilité.
- Prévoir les résultats réglementaires
- Assurer une veille réglementaire mondiale continue afin de détecter les changements et de diffuser des alertes en temps opportun pour permettre aux équipes d'anticiper l'évolution des exigences.
- En analysant les tendances historiques d'approbation, L'IA peut prévoir les décisions potentielles et mettre en évidence les zones à haut risque., permettant une planification proactive et une allocation optimale des ressources.
Cependant, l'IA générale ne constitue pas à elle seule une solution définitive. Bien qu'elle fournisse des informations précieuses, elle ne peut exécuter de manière autonome les flux de travail complexes et à plusieurs étapes qui caractérisent l'analyse des risques moderne. Pour transformer systématiquement les informations recueillies en actions conformes, les organisations doivent évoluer vers une IA agentielle, où des agents logiciels planifient, exécutent et adaptent les flux de travail sous la supervision humaine.
Si GenAI joue le rôle de catalyseur, l'IA agentique fonctionne comme une architecture de contrôle intégrée, reliant la détection, l'analyse, la rédaction, la notification et les pistes d'audit en une seule chaîne opérationnelle automatisée.
Le saut de l'agent : de la vision proactive à l'orchestration des flux de travail
IA agentique L'IA agentique désigne des agents logiciels orientés vers un objectif, opérant dans un cadre défini et capables de percevoir, de raisonner et d'agir au sein de systèmes interconnectés. Contrairement à l'IA générique, qui répond à des requêtes, l'IA agentique orchestre systématiquement des flux de travail pour atteindre des objectifs prédéfinis. Cela représente un changement fondamental, passant d'une automatisation passive à une exécution proactive.
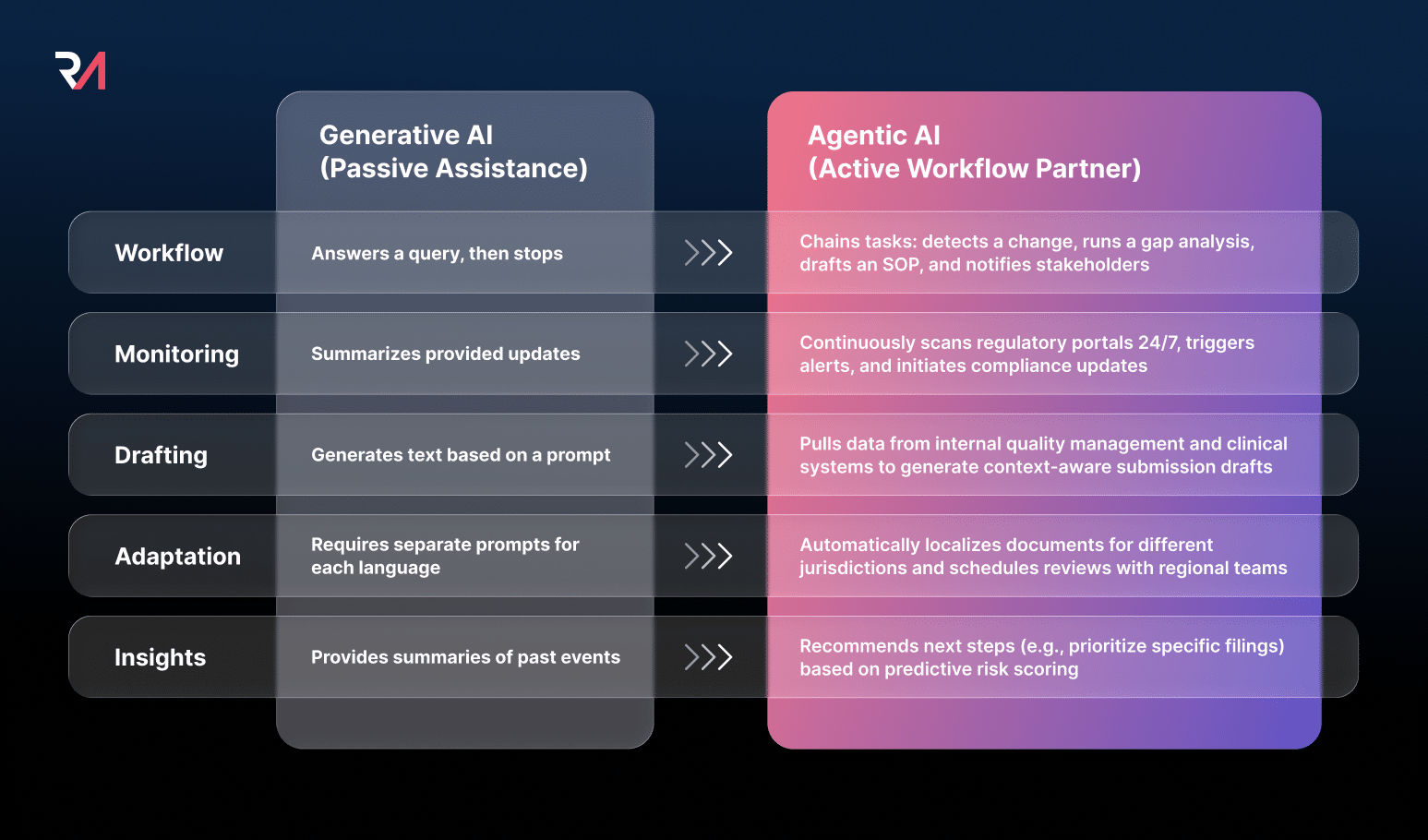
Cette évolution n'est pas un avenir lointain ; elle est déjà en cours. Les organisations qui adoptent l'IA proactive réduisent déjà leurs risques réglementaires, améliorent leur préparation aux audits et accélèrent leur accès au marché. Les projets pilotes suivants illustrent concrètement cet impact.
Projets pilotes d'IA agentique dans les affaires réglementaires : de la théorie à la pratique
Les études de cas pilotes suivantes sont des exemples illustratifs fondés sur les tendances sectorielles documentées et les analyses publiées concernant les flux de travail réglementaires pilotés par l'IA. Elles reflètent les thèmes communs relevés par les principales sources dans IA agentielle dans les sciences de la vie, discussions sur Automatisation des dossiers, et architectures multi-agents pour les affaires réglementaires. Ces exemples synthétisent les avantages observés, tels que la réduction des délais d'exécution, l'amélioration de la précision et le renforcement de la gouvernance, à partir de mises en œuvre concrètes décrites dans des rapports sectoriels et des articles de référence. Ils démontrent également comment les déploiements ciblés d'IA agentielle produisent des résultats mesurables.
Pilote A : Orchestration du changement d'étiquetage global
- Cas d'entreprise : Une entreprise pharmaceutique de taille moyenne a eu du mal à respecter un délai moyen de 10 jours pour les évaluations d'impact des changements d'étiquetage sur 25 marchés, ce qui a entraîné un taux de mises à jour manquées de 12%.
- Solution : Un flux de travail d'IA agentique a été déployé pour surveiller les sites web des autorités sanitaires, identifier les mises à jour relatives à l'étiquetage, effectuer une analyse d'impact initiale sur le portefeuille de produits de l'entreprise et rédiger des notes d'impact pour examen humain.
- Garde-fous : contrôles d’accès basés sur les rôles, suivi de la provenance des sources et révision bilingue obligatoire de tout contenu traduit automatiquement.
- Principaux cadres réglementaires et de qualité applicables : Ce projet pilote s’est déroulé à l’intersection de plusieurs grands cadres réglementaires et de qualité :
- Document ICH Q9(R1) Étape 4Gestion des risques qualité (adoptée en janvier 2023) : Ce document encadre l’utilisation des scores et contrôles de risques issus de l’IA dans les processus de gestion des risques qualité, notamment les exigences d’objectivité, de minimisation de la subjectivité et de prise de décision fondée sur les risques. La logique d’évaluation de l’impact de l’IA dans ce projet pilote a été conçue en accord avec ses quatre axes d’amélioration clés.
- UE MDR (Règlement (UE) 2017/745) / UE IVDR (Règlement (UE) 2017/746+ MDCG 2025-6 : Lorsque le portefeuille de produits concerné comprenait des dispositifs médicaux ou des DIV, les modifications d’étiquetage et leurs évaluations d’impact étaient soumises aux obligations du règlement MDR/IVDR relatives à la documentation technique, aux instructions d’utilisation et à la surveillance post-commercialisation. Les lignes directrices MDCG de juin 2025 ont précisé que les outils d’examen d’étiquetage assisté par IA devaient satisfaire aux exigences de transparence et de supervision humaine prévues par le cadre réglementaire conjoint MDR/IVDR et la loi européenne sur l’IA.
- Directives de la FDA concernant l'étiquetage et PCCP : Pour les produits destinés au marché américain, les flux de travail de modification d'étiquetage assistés par l'IA sont régis par le cadre du Plan de contrôle des modifications prédéterminé (PCCP) de la FDA. Ce cadre exige que toute modification de l'étiquetage d'un dispositif effectuée par l'IA soit documentée, traçable et communiquée aux utilisateurs. Les résultats du système de contrôle de version et de rédaction de notes de service du projet pilote ont été structurés de manière à être compatibles avec les exigences de divulgation du PCCP. Référence : Recommandations de la FDA pour le PCCP.
- Résultats (étude pilote de 6 mois) :
- Le délai moyen d'impact de la note a été réduit par 40% (de 10 jours à 6 jours).
- Le nombre de mises à jour manquées est tombé à presque zéro (<1%).
- Les erreurs de contrôle de version dans les processus en aval ont diminué de 50%.
Pilote B : Automatisation de l'assemblage du dossier du module 1
- Cas d'entreprise : Une entreprise de génériques a rencontré des retards importants dans la constitution des dossiers du module 1 (par exemple, les formulaires régionaux, les lettres de présentation) en vue des soumissions, les cycles de retravail consommant plus de 30% du temps de l'équipe.
- Solution : Un agent a été formé pour remplir automatiquement les modèles spécifiques à chaque pays avec des données provenant de systèmes internes, assembler les documents PDF requis et les conditionner pour la soumission électronique (RPS/eCTD).
- Mesures de protection : validation stricte des modèles, signature humaine obligatoire avant finalisation et file d’attente des exceptions pour les exigences non standard. Résultats (projet pilote de 9 mois) :
- Le temps de cycle d'assemblage du module 1 a été réduit de 35% à 45%.
- Les travaux supplémentaires causés par des erreurs administratives ont été réduits par 30%.
La prochaine évolution du modèle opérationnel réglementaire : une exécution proactive grâce à l’IA
L'agentivité désigne la capacité d'agir de manière indépendante, de faire des choix et de contrôler ses propres actions. L'IA agentique transpose ce concept dans le domaine numérique. La science réglementaire a commencé à formaliser ce que cela signifie concrètement : FDA–EMA Principes directeurs des bonnes pratiques en matière d'IA dans le développement des médicaments (Janvier 2026) définir les systèmes d'IA en utilisant OCDE La formulation “ systèmes à base de machines conçus pour fonctionner avec différents niveaux d’autonomie et pouvant faire preuve d’adaptabilité après déploiement ” englobe directement les architectures agentielles. Loi européenne sur l'IA Elle concrétise davantage ce principe en classant les systèmes d'IA autonomes selon leur niveau de risque, et en imposant des obligations proportionnées en matière de transparence, de supervision humaine et de gouvernance du cycle de vie. ISO/IEC 42001:2023, la première norme internationale de système de gestion de l'IA, fournit le cadre de gouvernance organisationnelle, couvrant l'évaluation des risques liés à l'IA, l'analyse d'impact et l'amélioration continue, au sein duquel les déploiements d'agents doivent être structurés. Ses capacités axées sur les objectifs sont habilitées à agir au nom de l'organisation., exécuter des actions avec des paramètres définis et approuvés par l'humain.
L'IA agentique va au-delà de l'automatisation passive ; elle opère dans un cadre défini et contrôlé pour planifier, exécuter et adapter les tâches. Voici quelques exemples de la manière dont elle améliore les capacités mentionnées ci-dessus :
- Orchestration dynamique des flux de travail : au lieu de se contenter de répondre aux requêtes, l’IA agentique peut enchaîner les tâches : détecter une nouvelle réglementation → effectuer une analyse des écarts → rédiger une procédure opérationnelle standard (POS) mise à jour → notifier les parties prenantes. Les flux de travail agentiques enchaînés qui concernent des livrables réglementés (POS, documents de soumission, étiquetage) sont soumis à la validation des systèmes informatiques GxP (Référence : GAMP 5 | Guide GAMP IATout document opératoire standard (SOP) ou document de soumission généré ou modifié par l'agent constitue un enregistrement électronique réglementé, déclenchant FDA 21 CFR Partie 11 (États-Unis) et Annexe 11 des BPF de l'UE (exigences de l'UE).
- Surveillance continue et actions proactives : ce système peut analyser en continu les portails réglementaires, déclencher des alertes et même initier des mises à jour de conformité sans intervention manuelle. La surveillance réglementaire autonome, qui alimente les décisions de conformité, fait pleinement partie de son champ d’action. ICH Q9(R1) Gestion des risques liés à la qualité.
- Rédaction contextuelle : L’IA agentique peut extraire des données de plusieurs systèmes internes (par exemple, bases de données d’essais cliniques, systèmes qualité) afin de générer des ébauches de soumissions personnalisées. Lorsqu’une IA agentique accède à des bases de données d’essais cliniques pour générer le contenu d’une soumission, elle opère simultanément selon plusieurs cadres qui se chevauchent : ICH M8/eCTD v4.0, afin de régir la structure, les métadonnées et les exigences de traçabilité de tout contenu destiné à être soumis électroniquement; Document de réflexion de l'EMA sur l'IA Il est clairement indiqué que les modèles de langage génératifs utilisés pour rédiger les informations sur les produits ou les documents de soumission doivent être utilisés sous étroite supervision humaine, avec des mécanismes de contrôle qualité garantissant l'exactitude factuelle et syntaxique avant la soumission réglementaire ; lorsque des données cliniques ou au niveau du patient sont consultées, RGPD (Règlement (UE) 2016/679) et les régimes équivalents de protection des données imposent des obligations de minimisation des données, de limitation des finalités et de gouvernance de l'accès.
- Adaptation multilingue et spécifique au marché : il peut localiser automatiquement les documents pour différentes juridictions et planifier des révisions avec les équipes régionales. GAMP 5 Les exigences de validation s'appliquent à l'agent de localisation lui-même en tant que système informatisé GxP.
- Informations prédictives et prescriptives : Au-delà des prévisions, l’IA agentielle peut recommander les prochaines étapes (par exemple, prioriser certains dépôts, allouer des ressources) en fonction de l’évaluation des risques. Lorsque les scores de risque et les recommandations générés par l’IA influencent les décisions réglementaires, notamment la priorisation des soumissions, l’allocation des ressources en fonction des délais de conformité ou l’escalade des signaux en pharmacovigilance, ICH Q9(R1) est le cadre de qualité principal. Principes communs de bonnes pratiques en matière d'IA de la FDA et de l'EMA Dans le développement des médicaments, renforcez cela à travers le principe 2 (approche fondée sur les risques) et le principe 8 (gestion du cycle de vie), en indiquant que le niveau de validation, de surveillance et de garanties doit être adapté au contexte d'utilisation de l'IA et aux risques associés.
Il ne s'agit pas simplement d'automatisation ; c'est un changement fondamental vers l'efficacité et la valeur stratégique.
Les gains d'efficacité et stratégiques décrits ci-dessus s'inscrivent dans des limites non négociables que les organisations doivent intégrer dès le départ dans chaque déploiement d'IA agentielle :
- Les agents d'IA sont utilisés pour appuyer le travail réglementaire et scientifique, et non pour remplacer le jugement formel ou la responsabilité.
- Tous les résultats générés par l'IA, y compris les procédures opérationnelles standard, l'étiquetage et les documents de soumission, sont soumis à un examen et à une approbation humaine documentés avant d'être partagés avec les autorités sanitaires.
- Toute analyse prédictive produite par une IA agentique, telle qu'une évaluation de la probabilité d'approbation ou des actions anticipées des autorités sanitaires, est uniquement destinée à faciliter la prise de décision et ne constitue pas une prédiction définitive ou approuvée par les organismes de réglementation.
Les responsables des affaires réglementaires n'ont pas besoin d'attendre une transformation à l'échelle de l'entreprise. Ils peuvent commencer par identifier un flux de travail répétitif et à fort volume, comme la veille stratégique, la constitution de dossiers ou le suivi des modifications d'étiquetage, et tester une approche multi-agents au sein d'une seule gamme de produits ou d'un seul segment de marché. Définissez une période d'évaluation de 90 jours avec des indicateurs clairs : délai d'action, taux de mises à jour manquées et temps de travail de l'équipe réaffecté à des tâches stratégiques. Les organisations qui intègrent aujourd'hui l'IA multi-agents à leur modèle opérationnel réglementaire ne se contenteront pas de suivre le rythme de la complexité ; elles la transformeront en avantage concurrentiel. Une mise en œuvre ciblée n'est que le point de départ. Le déploiement à grande échelle de l'IA multi-agents exige une feuille de route de maturité, une architecture multi-agents et une gouvernance adaptée aux environnements réglementés. (Le prochain article de cette série examinera comment mettre en place ces trois éléments.)
Cet article prolonge Août 2025 Forum mondial discussion sur l'IA agentielle au-delà des opérations cliniques jusqu'à la fonction des affaires réglementaires (AR), “Prochaines étapes de l'intelligence artificielle : l'IA agentique.”

