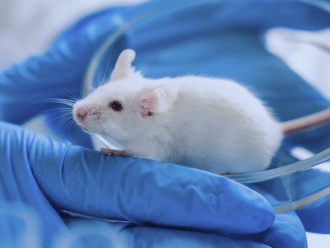
L'agence britannique de réglementation des médicaments et des produits de santé (MHRA) définit une voie réglementaire pour l'élimination progressive des tests sur les animaux…
Le 24 mars 2026, l’Agence de réglementation des médicaments et des produits de santé (MHRA) a introduit de nouveaux principes réglementaires pour les médicaments à usage humain…
En savoir plus
Le Japon met à jour la liste de contrôle d'auto-inspection de la JPMA pour la qualité…
Le 26 mars 2026, l'Association japonaise des fabricants de produits pharmaceutiques (JPMA) a publié une liste de contrôle révisée pour l'auto-inspection des tests de qualité…
En savoir plus
Restrictions de l'UE concernant les PFAS : l'ECHA lance une consultation du SEAC…
Le 26 mars 2026, l’Agence européenne des produits chimiques (ECHA) a lancé une consultation publique sur un projet d’avis publié par le Comité des affaires socio-économiques et sociales…
En savoir plus
L'agence brésilienne ANVISA fait le point sur les souches de vaccins contre la COVID-19, à faible risque…
Le 24 mars 2026, l'Agence nationale brésilienne de surveillance sanitaire (ANVISA) a annoncé une série de mises à jour réglementaires concernant la vaccination contre la COVID-19…
En savoir plus
La Turquie met à jour ses règles d'emballage et de notice d'information destinée aux patients…
L’Agence turque des médicaments et des dispositifs médicaux a publié des révisions substantielles de ses lignes directrices relatives aux informations sur l’emballage et aux informations destinées aux patients…
En savoir plus
Le ministère néerlandais de l'Économie et des Affaires économiques (MEB) introduit une obligation de déclaration pour…
Le 11 mars 2026, l’Agence néerlandaise d’évaluation des médicaments (MEB) a publié de nouvelles lignes directrices concernant les déclarations à l’intention des demandeurs d’autorisation de mise sur le marché d’un médicament duplex…
En savoir plus
La MHRA et le NICE lancent un processus d'autorisation et d'évaluation des technologies de la santé harmonisé…
Le 17 mars 2026, l’Agence de réglementation des médicaments et des produits de santé (MHRA) et l’Institut national pour l’excellence en matière de santé et de soins…
En savoir plus
La FDA, la MHRA et Santé Canada annoncent un symposium conjoint sur…
Le 10 mars 2026, la Food and Drug Administration (FDA) des États-Unis, en collaboration avec la Medicines and Healthcare products Regulatory Agency…
En savoir plus
L'EOF grecque rouvre sa plateforme de vérification d'authenticité…
Le 9 mars 2026, l'Organisation nationale des médicaments a annoncé la réouverture temporaire de sa plateforme de soumission numérique pour le déc…
En savoir plus
L’EMA ouvre les candidatures pour son portefeuille et ses technologies 2026…
Le 10 mars 2026, l’Agence européenne des médicaments (EMA) a annoncé que les candidatures aux réunions de portefeuille et de technologie (P…
En savoir plus